AIと実験データの融合で生命科学に革命!名城大学が「ROCKET」法を開発
タンパク質の立体構造を解き明かすことは、私たちの体を形作る生命の仕組みを理解し、病気の原因を探り、新しい薬を開発する上で非常に重要なステップです。しかし、この構造を正確に特定する作業は、これまで多くの時間と労力を要する困難なものでした。
そんな中、名城大学農学部の奥村裕紀教授を中心とする国際共同研究チームが、AI(人工知能)の力を最大限に活用し、この課題を劇的に解決する新手法「ROCKET」法を開発しました。この画期的な技術は、従来のタンパク質構造決定プロセスを根底から変え、生命科学の未来を大きく拓く可能性を秘めています。
タンパク質構造決定の重要性と従来の課題
タンパク質は、生命活動のほとんどすべてを担う重要な分子です。例えば、病原体を攻撃する免疫機能、体の動きを司る筋肉の収縮、食べ物を消化する酵素の働きなど、あらゆる生命現象に深く関わっています。これらの機能は、タンパク質がどのような「立体構造」をしているかによって決まります。まるで鍵と鍵穴のように、特定の形をしたタンパク質だけが特定の分子と結合し、その役割を果たすのです。
そのため、病気の治療薬を開発する際には、病気の原因となるタンパク質の構造を正確に把握し、その構造に合った薬を設計する必要があります。しかし、タンパク質の構造は非常に複雑で、原子レベルでその形を特定するには、X線結晶構造解析やクライオ電子顕微鏡といった高度な実験技術が不可欠でした。
近年、Google DeepMind社が開発したAIタンパク質構造予測ツール「AlphaFold」の登場は、この分野に大きな進歩をもたらしました。AlphaFoldは、アミノ酸配列(タンパク質の設計図)から、そのタンパク質がどのような立体構造をとるかを高い精度で予測できるようになり、2024年にはノーベル化学賞を受賞するほど画期的な技術として注目されました。
しかし、AlphaFoldによる予測はあくまで「予測」であり、創薬研究などで求められる「原子レベルでの厳密な確からしさ」を保証するには、やはり実験データによる裏付けが不可欠です。これまでのプロセスでは、AlphaFoldの予測モデルを参考にしつつも、実験データとのわずかなズレを、研究者が膨大な時間をかけて手作業で修正・構築する必要がありました。この「AIの予測」と「実際の実験データ」の間に横たわる溝をどう埋めるかが、構造生物学における大きな課題となっていたのです。
「ROCKET」法とは?AIと実験データを直接融合する革新技術
名城大学の国際共同研究チームが開発した「ROCKET」法は、この長年の課題を解決する画期的なアプローチです。この手法の最大の特徴は、AIの予測能力と実験データを直接、かつ効率的に融合させる点にあります。
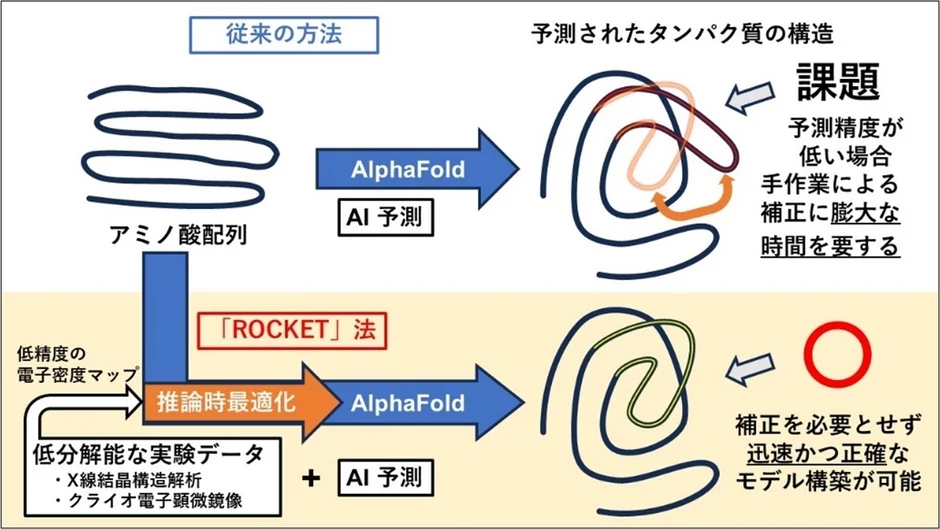
従来のプロセスでは、AIが予測した構造を「テンプレート」として使い、その後に実験データと照らし合わせて手作業で修正していました。例えるなら、AIが描いた絵(予測)を元に、実際の写真(実験データ)と見比べながら人間が修正するような作業です。
しかし、「ROCKET」法では、AlphaFoldの学習済みのAI(ニューラルネットワーク)自体を、実験で得られた電子密度マップ(タンパク質内の電子の分布を示す3次元の地図)に直接適合するように調整します。これは「推論時最適化(Inference-time optimization)」という技術を導入することで実現されました。
AIが持つ「タンパク質として物理的に正しい形」という膨大な事前知識(プライア)を保ちつつ、実験データが示す「目の前の具体的な事実」を反映したモデルを、AIが自動的に、かつ高精度に構築するのです。これにより、これまで研究者が手作業で行っていた修正作業が不要となり、構造決定のプロセスが劇的に高速化されます。
用語解説:AI初心者にもわかる専門用語
-
AlphaFold(アルファフォールド):Google DeepMind社が開発した、アミノ酸配列からタンパク質の立体構造を高い精度で予測できるAI。構造生物学に革命をもたらしました。
-
事前知識(Prior / プライア):AIや統計学の分野で使われる言葉で、新しいデータを見る前に、すでに持っている情報のことを指します。ROCKET法では、AlphaFoldが大量のタンパク質データから学習した「タンパク質として自然な形」という知識を、実験データを解釈する際の「ガイド」として活用します。
-
X線結晶構造解析:タンパク質の結晶にX線を当て、そのX線がどのように散乱するか(回折パターン)を解析することで、原子一つひとつの位置まで特定し、立体構造を明らかにする方法です。創薬研究で最も信頼されている標準的な手法の一つです。
-
クライオ電子顕微鏡:タンパク質などの生体分子を、非常に低い温度(クライオ)で急速に凍らせて、電子顕微鏡で観察する技術です。結晶化が難しいタンパク質でも、自然に近い状態で構造を調べることができ、近年急速に発展しています。
-
電子密度マップ:X線結晶構造解析やクライオ電子顕微鏡などの実験で得られる、タンパク質分子内の電子の分布を示した3次元の「地図」のようなものです。研究者はこの地図の中に、タンパク質を構成する原子のモデルを当てはめていくことで、正確な立体構造を決定します。
-
推論時最適化(Inference-time optimization):AIが学習した知識を使って「答えを出す(推論)」際に、手元にある特定のデータ(この場合は実験データ)に最も合うように、AI内部の計算を微調整する技術です。これにより、一般的な予測を、目の前の具体的な状況に合わせてカスタマイズすることができます。
ROCKET法の画期的な3つの特徴
ROCKET法は、これまでの構造生物学の常識を覆す、いくつかの画期的な特徴を持っています。
1. AIと実験データを直接結びつける「推論時最適化」
最も革新的なのは、AIの予測モデルと実験データを、まるで一体化させるかのように直接結びつける点です。従来のAIは、学習が終わるとその構造は固定され、新しいデータに対して「推論」を行うだけでした。しかしROCKET法では、AlphaFoldが学習した「化学的に妥当なタンパク質の形」という知識を保ちながら、実験で得られた電子密度マップに最も合うように、AIの内部構造そのものを調整します。
これにより、AIは「タンパク質は大体こんな形をしているはず」という知識と、「実験データが示す具体的な形」という事実を同時に考慮し、自動的に最適な構造モデルを構築できるようになります。これまで研究者が手作業で修正していた、予測と実測の間の細かなズレを、AIが自ら埋めてくれるようなものです。この「推論時最適化」というアプローチが、高速かつ高精度な構造決定を可能にする鍵となります。
2. 低品質なデータからでも高精度な構造解明が可能に
タンパク質の構造解析において、実験データの質は非常に重要です。特にX線結晶構造解析では、質の良い結晶を得ることが難しく、クライオ電子顕微鏡でも、常に高分解能なデータが得られるとは限りません。データ品質が低い場合、従来の解析手法では、そのデータから正確な構造を導き出すことが困難でした。
しかしROCKET法では、AIが持つ強力な「事前知識(プライア)」を活用することで、この問題を克服します。AIは、これまでに学習した膨大なタンパク質データから、「タンパク質が取りうる物理的に正しい形」という知識をすでに持っています。たとえ実験データがぼやけていたり、情報が少なかったりしても、AIはこの事前知識を「ガイド」として利用することで、足りない情報を補い、極めて正確な分子モデルを構築できるようになります。
これは、たとえ一部が隠れてよく見えない写真でも、その全体像を想像し、正確な形を推測できるベテランの職人のようなものです。低品質なデータしか得られないような難しいケースでも、高い信頼性を持つ構造モデルが得られることは、構造生物学研究の幅を大きく広げることにつながります。
3. 複雑な生体分子への応用を加速
生命現象に関わるタンパク質の中には、その構造が極めて複雑で、これまでの手法では解析が困難だったものが数多く存在します。例えば、奥村教授やカロリンスカ研究所のLuca Jovine教授らが長年研究してきた「受精に関わる複雑なタンパク質(ZP糖タンパク質など)」は、その代表例です。
これらの複雑な分子は、結晶化が難しかったり、不安定であったりするため、高分解能な実験データを取得することが非常に困難でした。しかし、ROCKET法を用いることで、低品質な実験データからでもAIの事前知識を借りて正確な構造を導き出せるため、これまで手つかずだったような難解な生体分子の構造解明が迅速かつ正確に行えるようになります。
この技術は、受精のメカニズム解明だけでなく、ウイルス感染、免疫応答、神経伝達など、様々な生命現象の根幹に関わる複雑なタンパク質の研究を大きく前進させることでしょう。
ROCKET法がもたらす未来:新薬開発と生命科学の加速
ROCKET法の確立は、構造生物学の解析プロセスを効率化し、高度化を同時に実現するものです。この技術がもたらす恩恵は計り知れません。
1. 構造決定の劇的な高速化
これまで数ヶ月から数年を要することもあった、特に難易度の高いタンパク質の構造決定が、ROCKET法を用いることで数時間から数日へと劇的に短縮されます。このスピードアップは、研究のサイクルを早め、より多くのタンパク質の構造を解明できるようになることを意味します。
2. 新薬開発の加速
病気の治療薬は、特定のタンパク質の構造を標的として設計されることが多いため、ターゲットとなるタンパク質の構造決定が迅速に行えるようになれば、新薬開発のプロセス全体が大幅に加速します。
例えば、新たな感染症ウイルスが出現した際、そのウイルスのタンパク質構造を素早く特定し、それに対応するワクチンや治療薬を短期間で開発することが可能になるでしょう。また、がん治療においても、がん細胞特有のタンパク質の構造を詳細に解析することで、より効果的で副作用の少ない標的薬の開発につながることが期待されます。
3. 未解明な生命現象の解明
これまで構造がわからなかった複雑なタンパク質の構造が解明されることで、これまで謎に包まれていた生命現象のメカニズムが次々と明らかになるでしょう。これは、基礎生命科学の発展に大きく貢献し、新たな発見や技術革新の土台となります。
ROCKET法は、まさに生命科学の基盤技術を刷新する、画期的な技術として大きな期待が寄せられています。
研究の背景と国際共同研究体制
この画期的な研究は、名城大学の奥村裕紀教授(生物化学、分子細胞生物学)が、スウェーデン・カロリンスカ研究所のLuca Jovine教授、イギリス・ケンブリッジ大学のRandy J. Read教授らと連携した国際共同研究チームによって行われました。
研究チームは、以下の3つの役割に分かれて研究を進めました。
- 理論・アルゴリズム開発:AIモデル(AlphaFold)を実験データと統合するための数学的フレームワークやプログラム開発を主導しました。ケンブリッジ大学のRandy J. Read教授や、AlphaFoldのオープンソース版「OpenFold」の開発者であるコロンビア大学のMohammed AlQuraishi助教授が中心となりました。
- 実験データの提供と検証:多様な生物学的サンプルとデータを提供し、ROCKET法によって得られる結果が生物学的に妥当であるかどうかの検証、および実際の実験データを用いた高度な解析・評価を実施しました。名城大学の奥村教授は、受精メカニズムに関連するタンパク質を用いた検証に貢献しました。
- 計算基盤・ツール支援:構造解析ソフト「PHENIX」の開発者であるロスアラモス国立研究所のThomas C. Terwilliger博士らが、計算基盤とツール開発を支援しました。
このように、世界中の著名な研究機関の専門家たちが協力し、それぞれの知見を結集することで、今回の画期的な成果が生まれました。
論文情報
本研究成果は、2026年4月1日(日本時間)に、英国の著名な科学誌『Nature Methods』にオンライン掲載されました。
-
雑誌名: Nature Methods
-
タイトル: AlphaFold as a prior: experimental structure determination conditioned on a pretrained neural network
-
著者名: Alisia Fadini,Minhuan Li,Airlie J. McCoy,Suresh Banjara,Hiroki Okumura,Eve Napier,Pietro Fontana,Amir R. Khan,Luca Jovine,Thomas C. Terwilliger,Randy J. Read,Doeke R. Hekstra,Mohammed AlQuraishi
-
掲載日時: 2026年4月1日
まとめ:ROCKET法が拓く生命科学の新たな地平
名城大学の奥村裕紀教授らが開発した「ROCKET」法は、AIの予測能力と実験データをこれまでにない形で融合させることで、タンパク質構造決定の効率と精度を飛躍的に向上させる革新的な技術です。この手法により、これまで解析が困難だった低品質な実験データからでも、高精度な構造モデルを導き出すことが可能になりました。
これにより、数ヶ月を要していた複雑なタンパク質の構造決定が数時間から数日へと短縮され、新薬開発や感染症対策、がん治療といった医療・ライフサイエンス分野に革命的な恩恵をもたらすことが期待されます。ROCKET法は、生命科学の発展を加速させ、私たちの健康と福祉に大きく貢献する可能性を秘めた、まさに未来を拓く技術と言えるでしょう。
研究チームは、今後「ROCKET」法をさまざまなタンパク質に適用し、タンパク質の機能異常に起因する疾患の理解をさらに深め、新たな治療法の開発につながることを期待しています。この技術の今後の展開に、世界中の研究者や関係者が大きな注目を寄せています。

